產(chǎn)品中心

本期看點(diǎn):
1、FDA拒絕批準(zhǔn)阿斯利康的Farxiga治療1型糖尿病。
2、哈佛科學(xué)家今天提供迄今為止最全面的證據(jù):素食可大幅降低2型糖尿病風(fēng)險(xiǎn)。
3、Midatech宣布其MidaCore金納米粒子糖尿病疫苗的首項(xiàng)人體研究安全性結(jié)果。
4.十二指腸黏膜重鋪術(shù)與血糖控制。
FDA拒絕批準(zhǔn)阿斯利康的Farxiga治療1型糖尿病

7月15日,美國(guó)FDA拒絕了Farxiga治療1型糖尿病(T1D)的補(bǔ)充新藥申請(qǐng)(sNDA)的批準(zhǔn)。FDA認(rèn)為,當(dāng)單獨(dú)使用胰島素不能提供足夠的血糖控制時(shí),SGLT2抑制劑Farxiga(達(dá)格列嗪)作為胰島素的輔助治療不能改善1型糖尿病患者的血糖控制。
在發(fā)布的聲明中,阿斯利康表示,已收到來(lái)自FDA針對(duì)該sNDA的一封完整回應(yīng)函(CRL),但沒(méi)有提供任何有關(guān)CRL的細(xì)節(jié)或重新提交申請(qǐng)的時(shí)間表,僅表示將與FDA密切合作討論下一步行動(dòng)。
另外除Farxiga外,今年3月,F(xiàn)DA以酮癥酸中毒(DKA)風(fēng)險(xiǎn)拒絕了賽諾菲/Lexicon合作開(kāi)發(fā)的SGLT-1/2雙效抑制劑Zynquista(sotagliflozin,索格列凈)的申請(qǐng)。
哈佛科學(xué)家今天提供迄今為止最全面的證據(jù):素食可大幅降低2型糖尿病風(fēng)險(xiǎn)

7月23日,美國(guó)哈佛大學(xué)T.H.Chan公共衛(wèi)生學(xué)院的發(fā)表在《JAMA Internal Medicine(美國(guó)醫(yī)學(xué)會(huì)內(nèi)科雜志)》上的一項(xiàng)新薈萃分析顯示,總體飲食模式堅(jiān)持以植物為主的人患2型糖尿病的風(fēng)險(xiǎn)比那些對(duì)飲食依從性較弱的人低23%。該研究還發(fā)現(xiàn),當(dāng)這種飲食模式中包括健康的植物性食物,如水果、蔬菜、全谷物、豆類和堅(jiān)果時(shí),這種聯(lián)系得到了加強(qiáng)。
在該研究中,研究人員確定了9項(xiàng)針對(duì)該關(guān)聯(lián)的研究,所有前瞻性觀察研究都檢測(cè)了18歲或以上成年人對(duì)基于植物飲食模式的依從性與2型糖尿病發(fā)病率之間的關(guān)系。他們的薈萃分析涉及307099名參與者的健康數(shù)據(jù),其中23544例患有2型糖尿病。他們分析了基于植物的飲食模式,其中包括健康的植物性食物,如水果、蔬菜、全谷物、堅(jiān)果和豆類,和不太健康的植物性食物,如土豆、白面粉和糖,以及少量的動(dòng)物產(chǎn)品。

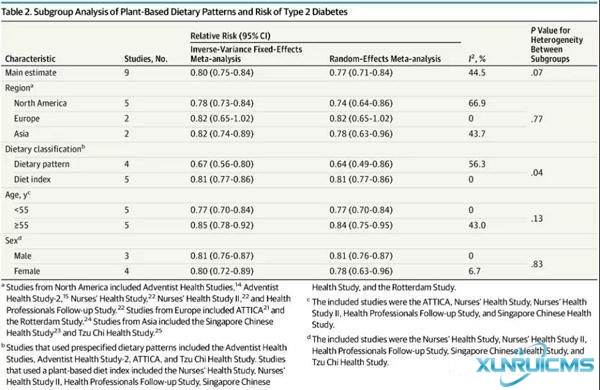
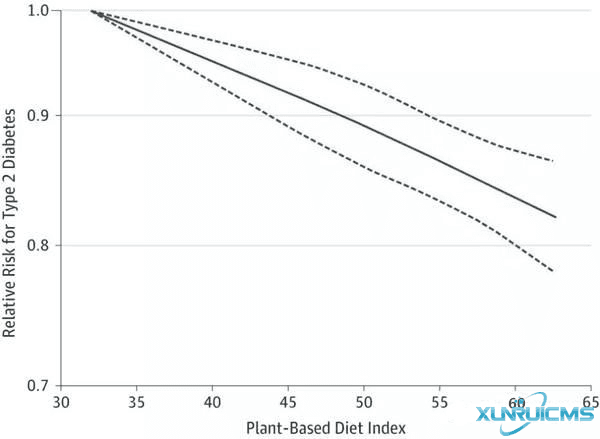
研究結(jié)果顯示,總體飲食模式堅(jiān)持以植物為主的人患2型糖尿病的風(fēng)險(xiǎn)比那些對(duì)飲食依從性較弱的人低23%。根據(jù)研究人員的說(shuō)法,可以解釋基于植物的飲食與降低2型糖尿病風(fēng)險(xiǎn)之間關(guān)聯(lián)的一種機(jī)制,是健康的植物性食物已被證明可以單獨(dú)或共同改善胰島素敏感性和血壓、減少體重增加,并減輕全身炎癥,而這些都是罹患2型糖尿病的潛在風(fēng)險(xiǎn)因素。
Midatech宣布其MidaCore金納米粒子糖尿病疫苗的首項(xiàng)人體研究安全性結(jié)果
第一階段研究的重點(diǎn)是評(píng)估MTX102的安全性。在5名符合嚴(yán)格遺傳參數(shù)的I型糖尿病患者被招募到研究中并接受該藥物治療。結(jié)果顯示MTX102耐受性良好,無(wú)癥狀的局部注射部位反應(yīng)是唯一與藥物相關(guān)的發(fā)現(xiàn),未報(bào)告嚴(yán)重不良事件。
MTX102是基于Midatech的超小金納米粒子藥物綴合物MidaCore技術(shù)平臺(tái)開(kāi)發(fā)的。在疫苗領(lǐng)域,MTX102代表了一種創(chuàng)新方法,利用金納米粒子的多功能特性,將免疫原性肽和耐受劑結(jié)合起來(lái),更有效地將它們傳遞給免疫細(xì)胞,從而抑制糖尿病等疾病的自身免疫反應(yīng)。
十二指腸黏膜重鋪術(shù)與血糖控制
近日研究人員評(píng)估了十二指腸黏膜重鋪術(shù)(DMR)對(duì)II型糖尿病的血糖的影響。
T2D(HbA1c 59~86 mmol/mol,7.5%~10.0%)患者(BMI 24-40)在穩(wěn)定口服降糖藥物的基礎(chǔ)上接受DMR治療。降糖藥物在DMR后繼續(xù)治療24周。隨訪期間,測(cè)定HbA1c、空腹血糖(FPG)、體重、肝轉(zhuǎn)氨酶、胰島素抵抗穩(wěn)態(tài)模型評(píng)估(HOMA-IR)、不良事件(AES)和治療滿意度。
46例患者中,37例(80%)接受了完整的DMR,36例納入分析。24例患者發(fā)生至少1例與DMR相關(guān)的AE(52%),其中81%為輕度。報(bào)告了1起SAE,未報(bào)告非預(yù)期AE。24周DMR(n=36)后,患者HbA1c(-10mmol/mol,0.9%)、FPG(-1.7)、HOMA-IR均有改善(-2.9)、體重 (-2.5 kg)以及肝轉(zhuǎn)氨酶水平均有所降低。效果在12個(gè)月內(nèi)維持。HbA1c的變化與輕度體重減輕無(wú)關(guān)。糖尿病治療滿意度評(píng)分顯著提高。
